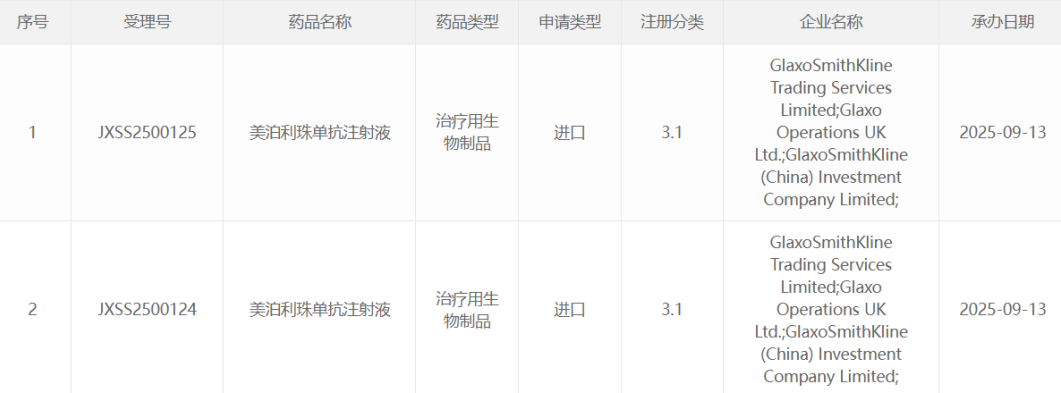
2025年9月13日,国家药品监督管理局药品审评中心(CDE)网站显示,葛兰素史克(GSK)旗下全球首创的IL-5单抗美泊利珠单抗提交了新适应症的上市申请。据临床开发进度推测,此次申报的新适应症可能为慢性阻塞性肺病(COPD)。
美泊利珠单抗:IL-5单抗的先锋者
美泊利珠单抗是一款由GSK开发的全球首创IL-5单抗,每月一次的注射频率大大简化了患者的用药流程。2011年首次研发成功后,美泊利珠单抗已覆盖多项呼吸相关疾病:
2021年11月:首次在国内获批上市,用于治疗嗜酸性肉芽肿性多血管炎(EGPA)。
后续扩展:获批治疗嗜酸性粒细胞性重度哮喘和慢性鼻窦炎伴鼻息肉,为2型炎症相关疾病患者提供了更多选择。
COPD适应症:2型炎症患者的福音
慢性阻塞性肺病(COPD)是仅次于心血管疾病和癌症的全球第三大死亡原因,全球患者人数约为3.9亿。然而,这种疾病的诱因复杂,约40%的患者是由2型炎症反应推动,其特征是血嗜酸性粒细胞水平升高。对这种亚型患者的靶向治疗需求尚未完全满足。
今年5月,美泊利珠单抗已获美国FDA批准用于附加维持治疗嗜酸性粒细胞表型的COPD,成为首个获批COPD适应症的IL-5药物,也是COPD治疗领域的首个可每月给药的生物制剂。
III期MATINEE研究:验证疗效与安全性
美泊利珠单抗在COPD适应症的获批过程中,其临床疗效基于III期MATINEE研究的数据:
研究设计:一项多中心、随机、双盲安慰剂对照研究,招募806名中重度COPD患者。这些患者均存在以血嗜酸性粒细胞升高为特征的2型炎症并经历过疾病的频繁急性加重。
治疗方案:美泊利珠单抗每4周皮下注射100mg,作为维持治疗的附加方案。
研究终点:研究主要评估了中重度COPD年恶化率的减少情况。
关键结果:
治疗104周后,美泊利珠单抗组的年恶化率显著低于安慰剂组(0.80 vs 1.01,P=0.01),表明该药有效降低了COPD急性加重的发生频率。
同时,美泊利珠单抗的安全性表现良好,与既往适应症中的研究一致。
美泊利珠单抗国内进展
2021年,GSK在国内启动了美泊利珠单抗治疗嗜酸性粒细胞相关COPD的III期研究(CTR20210176),该研究于今年9月显示完成。这为此次新适应症的申报奠定了坚实数据基础。作为2型炎症COPD患者的一种重要选择,美泊利珠单抗有望帮助缓解疾病恶化、改善患者生活质量。
总结:美泊利珠单抗创新药物再升级
美泊利珠单抗的新适应症申报若能获批,意味着该药将在呼吸系统疾病治疗领域迈出重要一步,为COPD领域的2型炎症患者提供新的治疗选择。随着未来医疗需求的逐步扩大,这款每月一次给药的生物制剂,将进一步填补国内呼吸系统疾病靶向治疗的空白,为患者带来更多的希望。