近日,中山大学器官移植中心何晓顺教授、郭志勇教授团队联合生命科学院邝栋明教授团队,通过多维数据分析,揭示了乙肝相关慢加急性肝衰竭(ACLF)的关键病理机制。这一研究成果发表在《肝病学》(Hepatology)期刊上,为ACLF的精准诊疗提供了新思路。
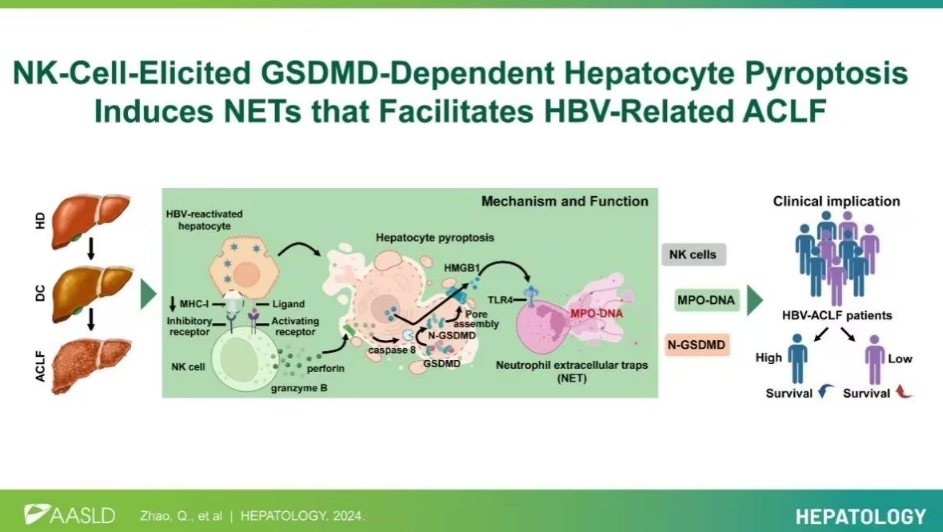
肝细胞焦亡是乙肝相关ACLF的核心病理
研究团队在正常肝脏、乙肝病毒(HBV)相关肝硬化和ACLF患者病变组织中,进行了高分辨率转录组测序和组织原位染色分析,发现 肝细胞焦亡 是HBV相关ACLF患者肝组织中的主要细胞死亡形式。
进一步研究表明,HBV的再激活引起肝细胞中MHC-I分子的表达缺失,这一机制触发了细胞毒性自然杀伤(NK)细胞的异常活跃。NK细胞通过分泌穿孔素和颗粒酶,依赖GSDMD/Caspase-8通路,最终引发了肝细胞焦亡。从机制上看,这一病理事件是HBV相关ACLF发展的核心驱动因素。
中性粒细胞在肝细胞焦亡中的作用
肝细胞焦亡不仅直接导致肝脏损伤,还释放了高迁移率族蛋白B1(HMGB1),进一步加剧了炎症反应。研究发现,焦亡肝细胞释放的HMGB1能够招募中性粒细胞聚集到肝组织病变区域。更为重要的是,这种聚集的中性粒细胞会释放网状结构物(NETs),进一步加速了肝组织的疾病进展。
MPO-DNA作为预后标记的新发现
为了探索潜在的临床标记物,研究团队聚焦于NETs的血浆标记物。其中,MPO-DNA(髓过氧化物酶-DNA复合物)的水平与患者的预后呈显著负相关。研究证实,HBV相关ACLF患者血浆中MPO-DNA水平越高,患者的生存率越低。这一发现为临床提供了有价值的预后评估工具。
创新研究:体外模型验证新治疗方向
研究者还采用了独特的常温机械灌注体外病肝养护模型,进一步验证了抑制肝细胞焦亡对疾病控制的效果。通过阻断GSDMD依赖的焦亡机制,成功减少了HMGB1的释放,从而显著抑制了NETs的生成。这一结果表明,通过选择性干预焦亡通路及其相关炎症环境,有望为HBV相关ACLF提供一种全新的治疗策略。
临床启示:调节焦亡与免疫微环境的新路径
研究揭示了GSDMD依赖的焦亡在ACLF病程中的核心作用,并将这一机制与NETs形成、肝衰竭预后关联起来。选择性干预肝细胞焦亡和调控中性粒细胞反应的新疗法,不仅有助于预防肝脏进一步受损,还为改善患者的临床存活率提供了强有力的作用机制支持。
结语:开启HBV相关ACLF治疗的新希望
本项研究填补了在HBV相关ACLF机制研究中的关键空白。通过解析肝细胞焦亡及其免疫调控作用,研究团队为疾病的诊断与治疗提供了前所未有的新靶点。结合MPO-DNA等预后标记物与焦亡机制的联合研究,有望推动未来针对ACLF的精准干预策略,更好地保护患者肝功能,改善疾病预后。