Cogent Biosciences, Inc.近日发布了Bezuclastinib联合舒尼替尼治疗伊马替尼耐药或不耐受的胃肠道间质瘤(GIST)患者的III期临床试验PEAK的积极数据。此次结果被认为是20多年来针对二线GIST患者的首个阳性III期临床试验,并可能为这类患者的治疗带来新的标准。

Bezuclastinib的作用机制
Bezuclastinib是一种选择性酪氨酸激酶抑制剂,主要针对KIT D816V突变以及KIT第17号外显子上的其他突变,从而有效抑制这些突变引发的肿瘤生长。其临床应用为GIST患者提供了新的治疗选择,尤其是对于那些对传统治疗(如伊马替尼)产生耐药或无法耐受的患者。
PEAK试验设计与结果
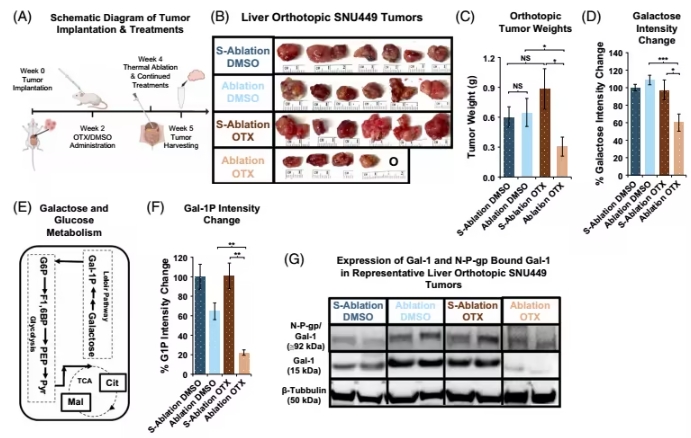
PEAK试验是一项全球多中心、随机III期临床试验,旨在比较Bezuclastinib联合舒尼替尼与舒尼替尼单药治疗在伊马替尼耐药或不耐受的GIST患者中的疗效和安全性。根据截至2025年9月30日的数据,主要结果显示Bezuclastinib联合舒尼替尼疗法在无进展生存期(PFS)这一主要终点上,展现出显著的临床获益。与标准治疗相比,疾病进展或死亡的风险降低了50%(风险比为0.50)。
无进展生存期(PFS):Bezuclastinib联合治疗的中位PFS为16.5个月,而舒尼替尼单药治疗组为9.2个月。
客观缓解率(ORR):对于伊马替尼耐药患者,Bezuclastinib联合疗法的客观缓解率达到46%,而舒尼替尼单药治疗组为26%。
总生存期:截至本次分析时,总生存期数据尚未完全成熟。
安全性评估
在安全性方面,Bezuclastinib联合舒尼替尼的总体耐受性良好。与舒尼替尼的已知安全性相比,Bezuclastinib联合疗法未显示出独特的风险,表明其在安全性方面与现有治疗方案相当。
下一步计划
基于这些积极的数据,Cogent预计将在2026年上半年向FDA提交Bezuclastinib用于治疗伊马替尼耐药或不耐受的GIST患者的上市申请。此外,PEAK III期试验的完整数据分析仍在进行中,Cogent计划在2026年上半年即将举行的科学会议上公布更多详细的研究结果。
通过这项研究,Bezuclastinib联合舒尼替尼的疗法可能为GIST患者提供一个新的治疗选择,尤其是那些对现有治疗方法反应不佳的患者。