泽璟制药DLL3/CD3三特异性抗体ZG006拟纳入突破性疗法,聚焦小细胞肺癌创新治疗
 搜医药
搜医药
关键词: #健康资讯
 搜医药
搜医药
关键词: #健康资讯
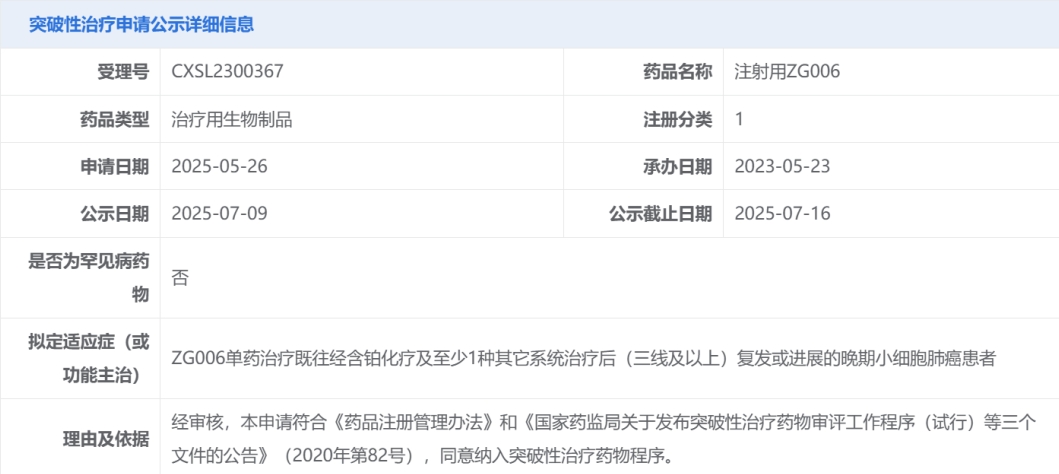
7月9日,国家药品监督管理局药品审评中心(CDE)官网发布消息,泽璟制药研发的三特异性抗体药物ZG006拟被纳入突破性疗法认定,用于单药治疗经过含铂化疗及至少一种其他系统治疗(三线及以上)后复发或进展的晚期小细胞肺癌(SCLC)患者。作为一款全球首创(First-in-Class)药物,ZG006在小细胞肺癌领域抢占先机,展现了显著的治疗潜力。
ZG006设计机制:精准杀伤癌细胞
ZG006是泽璟制药与旗下子公司Gensun Biopharma联合研发的DLL3/CD3三特异性T细胞衔接器(TCE)。这种全新的抗体设计可以通过以下方式高效杀伤肿瘤细胞:
双抗DLL3作用:
抗DLL3端同时结合肿瘤细胞表面不同的DLL3表位,精准识别癌细胞的特异性标志。DLL3是一种在小细胞肺癌中高表达的靶点,而在正常组织中表达极低,因此为增强靶向治疗效果提供了基础。
抗CD3连接T细胞:
ZG006的一端通过CD3结合T细胞,将T细胞高效引导至肿瘤微环境(TME),促进肿瘤浸润。
激活T细胞杀伤:
通过增强T细胞与肿瘤细胞的物理接触,诱导T细胞释放细胞毒性分子,有效消灭肿瘤细胞。
扎实的临床前数据:肿瘤显著抑制并完全消退
在临床前研究中,ZG006在小鼠肿瘤模型上展示了其强大的抗肿瘤活性。研究发现,ZG006能够显著抑制肿瘤生长,并使较大比例的小鼠肿瘤完全消退。这一结果表明ZG006具有潜力成为一种强效的实体瘤免疫治疗工具。
ZG006的研发成果已获得广泛认可,目前该药物不仅获得了美国FDA和中国NMPA的临床试验许可,还被美国FDA授予孤儿药资格认定。
II期研究:显著疗效与安全性初现
在2025年的美国临床肿瘤学会(ASCO)年会上,泽璟制药公布了ZG006的临床试验进展及II期研究数据:
试验设计:
该研究评估ZG006单药(10mg或30mg剂量,每两周一次)治疗既往接受至少二线系统治疗的晚期小细胞肺癌患者的疗效和安全性。
疗效数据:
入组情况:试验共计纳入40例患者,其中27例具有可评估疗效的数据。
总体疗效:整体客观缓解率(ORR)达到66.7%(18/27),疾病控制率(DCR)为92.6%。
分剂量情况:
10mg剂量组ORR为53.8%(7/13),DCR为84.6%(11/13);
30mg剂量组ORR高达78.6%(11/14),DCR为100%(14/14)。
DLL3低表达患者疗效:
在DLL3低表达(17例)及中表达(4例)患者中,ORR达到71.4%(15/21),进一步验证了ZG006在不同DLL3表达水平患者中的普适疗效。
无进展生存期(PFS)与缓解持续时间(DoR):
DoR与PFS数据尚未成熟,后续随访将揭示更完整的疗效数据。
安全性数据:耐受性良好,副作用可控
安全性结果:
在所有治疗患者中,治疗相关不良事件(TRAE)发生率为87.5%(35/40),3级及以上TRAE出现率为12.5%(5/40)。
SAE(严重不良事件)发生率为12.5%(5/40),未发现因TRAE导致的治疗中断或死亡病例。
耐受性良好:
总体来看,ZG006在安全性方面表现良好,未出现影响治疗持续性的严重毒性问题。
DLL3:小细胞肺癌的新靶点
DLL3作为Notch信号通路的关键调控分子,其高选择性表达特性使其成为小细胞肺癌的重要靶点。DLL3的独特性质不仅降低了脱靶毒性的风险,也为发展针对性更高的治疗方案提供了可能性。ZG006基于DLL3的双重靶向机制,尤其在DLL3低表达患者的疗效表现,展示出了多方面潜力。
展望未来:ZG006或成为SCLC治疗里程碑
ZG006作为一款三特异性抗体药物,兼具T细胞招募与精准靶向肿瘤表位的能力,其临床数据已初步展现了强大的抗肿瘤效果和良好的安全性。如果后续研究继续验证其疗效,ZG006有望填补晚期小细胞肺癌治疗的空白,并成为国际抗体工程与肿瘤免疫领域的重要突破产品。
在现有小细胞肺癌治疗选择相对有限的情况下,ZG006的出现无疑为患者带来了新的选择和希望。随着其申请被纳入突破性疗法及研究数据的进一步披露,ZG006将在肿瘤治疗领域能否迎来全新突破值得期待。
2025-12-27

2025-12-27

2025-12-27

2025-12-27

2025-12-27