拓舒沃(Tibsovo)依维替尼国内有没有上市

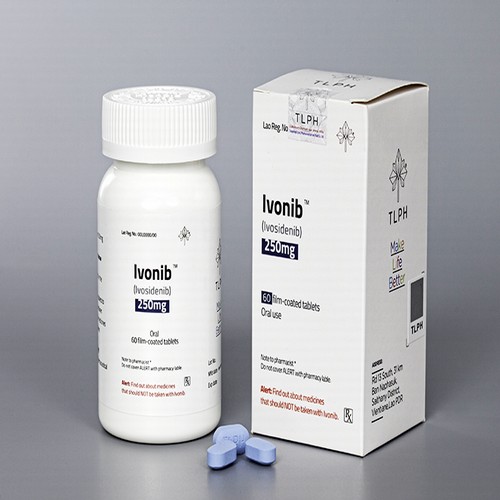
拓舒沃(Tibsovo)依维替尼国内有没有上市,拓舒沃(Ivosidenib)最早于2018年7月20日在美国首次全球获批。目前在国内已经上市,于2022年2月9日获得国家药品监督管理局(NMPA)的批准。
拓舒沃(Tibsovo)依维替尼是一种用于治疗特定类型白血病的药物,其在国内的上市情况引发了业内的广泛关注。本文将对拓舒沃的用途、国内上市信息、与艾伏尼布(Ivosidenib)的对比以及对患者的影响进行探讨。
1. 拓舒沃的药物背景
拓舒沃(Tibsovo)是一种靶向药物,主要用于治疗急性髓系白血病(AML),尤其是针对携带IDH1突变的患者。它的作用机制是通过抑制IDH1酶的活性,减少肿瘤细胞的增殖,从而帮助改善患者的预后。
2. 国内上市情况
截至目前,拓舒沃在中国的上市进程仍在进行中。根据相关的药品审批信息,该药品正处于临床试验阶段,具体的上市时间尚未确定。对于许多患者而言,及时获得有效的治疗手段是至关重要的,因此其上市状况备受关注。
3. 与艾伏尼布的对比
艾伏尼布(Ivosidenib)同样是一种针对IDH1突变的靶向药物,已在多个国家获得批准。两者在治疗机制上相似,但在临床疗效、适应症及副作用方面可能存在差异。比较两者的治疗方案,对于医生制定个性化治疗计划具有重要意义。
4. 对患者的影响
拓舒沃的上市将为IDH1突变的急性髓系白血病患者提供新的治疗选择。有效的靶向治疗能够提高患者的生存率,减轻病痛,改善生活质量。同时,药物的价格、可及性及医疗资源的分配也将直接影响患者的受益。
拓舒沃依维替尼在国内的上市情况令人期待,随着临床试验的推进和监管部门的审批,我们有望在不久的将来看到这一重要药物为更多患者带来新的治疗机会。希望未来能够有更多有效的药物上市,为白血病患者提供更加多元化和精准的治疗方案。